What works in managing complex conditions in older people in primary and community care? A state‐of‐the‐art review
Rachael Frost, Health Soc Care Community. 2020 Jul 15. PMID: 32671922
マルモ連載がおかげさまで、少しずつ注目されています。
【新連載】近年増加する多疾患併存(マルチモビディティ)のケースに対して,家庭医療学の視点からのアプローチを学びましょう。/週刊医学界新聞〔連載〕ケースで学ぶマルチモビディティ(1) マルモの診かた総論(前編)(大浦誠)https://t.co/MQ6QWYWCXL pic.twitter.com/EZQb73ZtcD
— 週刊医学界新聞 (@igakukaishinbun) 2020年4月13日
http://www.igaku-shoin.co.jp/paperDetail.do?id=PA03367_05
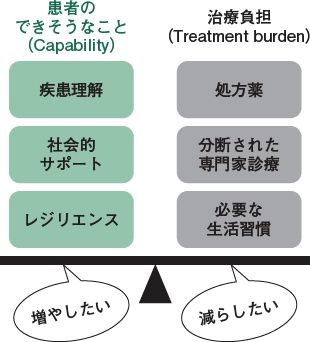
私はこの連載でバランスモデルというものを中心に解説していますが
多疾患併存を管理するためにどんなモデルが有効なのかをまとめたレビューが2020年7月15日に発表されたので、ここでまとめてみます。
概要
複雑な健康状態で生活している高齢者の数は増加しており、これらの大部分はプライマリ・ケアおよび地域社会の環境で管理されています。多くのケアモデルがそれらをサポートするために開発されてきましたが、それらの価値についてはさまざまなエビデンスがあり、それらには複数の重複するコンポーネントが含まれています。私たちは、プライマリーケアとコミュニティケアで高齢者の複雑な状態を管理するために何が機能するかを学ぶためのエビデンスを統合することを目指しました。系統的レビューの最先端のレビューを実施しました。2009年1月から2019年7月までの3つのデータベースで、認知症などの高齢者に共通する慢性疾患、フレイル、多疾患併存、複雑な神経学的状態のプライマリケアとコミュニティケアのモデルを検索しました。各モデルタイプのエビデンスを要約し、有効性に影響を与えたコンポーネントを特定するために、レビュー結果を説明的に合成しました。2,129のユニークなタイトルとアブストラクトのうち、178の全文がレビューされ、54の系統的レビューが含まれていました。ケアのモデルは、身体的健康やサービス利用の結果よりも抑うつ症状とメンタルヘルスの結果を改善する可能性が高いことがわかりました。自己管理、患者教育、フォローアップケア手順による評価、構造化されたケアプロセスまたは経路を含む介入は、有効性のより大きなエビデンスを示しました。医療サービス統合のレベルは、チームに特定の専門家タイプを含めることよりも重要であるように見えました。しかし、経験豊富で資格のある看護師は、より良い結果と関連していた。これらの結論は、レビュー間の重複、一部の含まれるレビュー内の投票数への依存、および調査レポートの質によって制限されます。結論として、高齢者の複雑な状態に対するプライマリ・ケアおよびコミュニティ・ケアの介入は、以下を含むべきである。(a)明確な介入目標、(b)明確な理論的根拠、(c)自己管理と患者教育、医療専門家間の構造化された連携、専門家支援の要素。介入における最適な強度、長さ、チーム構成、テクノロジーの役割を決定するためのさらなる研究が必要です。
このトピックについて何がわかっていますか?
1つ以上の長期的な状態で生活する高齢者の数は増加しています
この人口は、プライマリおよびコミュニティケアの設定で管理されることが多い
この設定には複数のケアモデルが存在しますが、これらには重複するコンポーネントがあり、有効性のエビデンスが混在しています
この論文で何が追加されますか?
プライマリおよびコミュニティケアモデルは、うつ症状やその他のメンタルヘルスの結果を改善する可能性が最も高いです。
自己管理、患者教育、フォローアップケア手順による評価、構造化されたケアプロセスまたは経路を含む理論ベースの介入が効果的である可能性が高い
チームの統合の程度はチーム構成よりも重要であるように見えますが、資格のある看護師の数が多いほど結果が良くなります
1背景
平均寿命および高齢化人口の世界的な増加に伴い、特に85歳以上の人々の間で、長期条件(long‐term conditions:LTC)で生活する高齢者の数が増加しています。LTCは一般に治癒することはできませんが、多くの場合、2型糖尿病、慢性閉塞性肺疾患(COPD)、うつ病などの薬物療法や他の治療法(Department of Health、2012年)によって症状を抑えることができ ます。イギリス(UK)の60歳以上の高齢者のうち、58%がLTCと一緒に住んでおり、25%が2つ以上の疾患(多疾患併存)で暮らしており、これらの割合は年齢によって大幅に上昇しています(Department of Health、 2012年)。多くの場合、LTCの数値には、フレイルなどの高齢者に一般的な他の状態が含まれません(11%; Collard、Boter、Schoevers、およびOude Voshaar、 2012)、認知症(7%; Princeら、 2014)、パーキンソン病(1%; Tysnes&Storstein、 2017)、または脳卒中(2%; Bhatnagar、Wickramasinghe、Wilkins、およびTownsend、 2016)。「複雑な患者」の定義についてコンセンサスはありませんが、定義は通常、複数の相互作用する状態と、健康や健康システムの社会的決定要因などの状況要因で構成されます(Manning&Gagnon、 2017年)。このレビューでは、1つまたは複数のLTCが住んでいる高齢者を、プライマリおよびコミュニティのヘルスケア環境で管理されていると定義しました。
従来、ヘルスケアシステムは、LTCではなく急性状態を診断および治療するように構成されてきたため、高齢者のニーズを反映していません(World Health Organisation、2015年)。専門医療ではなくプライマリケアやコミュニティケアにケアをシフトすることで、家の近くでより包括的な医療を提供し、複数の専門家の意見を活用することもできます。ケアのモデルは、統合ケア、共同ケア、慢性ケアモデルなどのプライマリおよびコミュニティケアにおける複雑なLTCを管理するために開発されました(WHO、 2016年)。過去20年間、これらのモデルは試験とレビューで広く評価されてきましたが、高齢者ではさまざまな結果が示されています(van Eck van der Sluijs et al。、 2018 ; Mitchell et al。、 2015)。さらに、これらのモデルは明確に説明されることが多いですが、通常、エビデンスに基づくケアプロトコルの使用、患者の自己管理の促進、医療従事者間のコラボレーションの改善など、重複する要素があります。どのコンポーネントが効果的であるかは特定されていませんが、レビューの概要の1つでは、高齢者向けの統合ケアの既存モデルの重要な要素は、集学的チームケア、包括的な評価、ケース管理(Briggs、Valentijn、Thiyayagarajan、およびAraujo De)であることがわかりましたCarvalho、 2018年)。その他のレビューでは、主に実装の障壁と促進者に焦点が当てられています(Threapleton et al。、 2017)。その結果、異なるモデル間で何がうまく機能しているかを特定することができる潜在的な共通点がある。高齢者の健康管理はプライマリ・ケアで行われることが多くなってきており、この最先端のレビューの目的は、プライマリ・ケアとコミュニティ・ケアのモデルに関するシステマティック・レビューから、複雑なLTCのニーズを持つ高齢者を管理するために、このような環境で何が最も効果的なのかについての重要なメッセージを引き出すことである。
2方法
我々は、高齢者の複雑な状態の一次管理と地域管理の効果的な要素を特定するために、システマティックレビューの最先端のレビューを実施した。最先端のレビューは、最新のエビデンスのナラティブ合成に焦点を当てており、将来の研究の知識と優先順位の現在の状態を概説し、正式な品質評価は含まれていません(Grant&Booth、 2009)。品質を評価するつもりはなかったので、利用可能な最高品質のエビデンスを独自に選択するために体系的なレビューのみを含め、このトピックについて過去10年間に完了した体系的なレビューに焦点を当てました。古くなっている(古い試験が後のレビューに含まれている)か、または置き換えられました。系統的レビューは、構造化された検索戦略、スクリーニングプロセス、品質評価、およびナラティブまたは定量的合成を使用するレビューとして定義されました。データベースのレビューフィルターを使用して、条件、プライマリおよびコミュニティのケア、介入のタイプに基づく包括的な検索用語を使用して、Medline、Embase、Cochrane Database of Systematic Reviews(2009年1月1日から2019年7月1日)の検索からレビューを特定しました(付録S1を参照)。
RFは、Box 1の基準に従って、Rayyanソフトウェア(Ouzzani et al。、2016) を使用して、すべてのタイトル、要約、および全文をレビューしました。 、10%がAWによって独自にチェックされ、意見の相違は上級チームメンバーとの話し合いまたは相談を通じて解決されました。RFは、各レビューからデータを簡潔な単純な形式で抽出しました。これには、レビュー特性に関する項目、関連セクションがレビュー全体であるかサブグループ分析であるか、対象となる主な条件、ケアのモデルおよびコンパレーターが含まれていました(s)対象、レビュー著者によって報告された対象研究の質の要約、ケアモデルの全体的な証拠、および(a)介入を提供する必要のある人に関する各レビュー(報告されている場合)の証拠(b)介入の接触頻度、持続時間と強度、(c)全体の介入持続時間、(d)接触のタイプ(例:対面)、(d)医療専門家の場所、地域のサービスとの適合性、(e)学際的な関与、(f)対象となる介入機能、および(g)対象となる介入ドメイン。結果は、モデルのタイプと条件に従って表にまとめられ、コンポーネントに関する主要なメッセージが表に抽出されました。対象国、対象条件、レビューに含まれる試験の質、および各モデルで利用可能な証拠の量を記述的に要約しました。エビデンスは、レビュー全体で構成要素の一貫したエビデンス、矛盾するエビデンスと効果がないことに関するエビデンス、およびこれらをコンテキスト化するための介入、条件、設定に基づいて、主要なメッセージを作成するために、レビュー全体でナラティブに合成されました。対象国、対象条件、レビューに含まれる試験の質、および各モデルで利用可能な証拠の量を記述的に要約しました。エビデンスは、レビュー全体で構成要素の一貫したエビデンス、矛盾するエビデンスと効果がないことに関するエビデンス、およびこれらをコンテキスト化するための介入、条件、設定に基づいて、主要なメッセージを作成するために、レビュー全体でナラティブに合成されました。対象国、対象条件、レビューに含まれる試験の質、および各モデルで利用可能な証拠の量を記述的に要約しました。エビデンスは、レビュー全体で構成要素の一貫したエビデンス、矛盾するエビデンスと効果がないことに関するエビデンス、およびこれらをコンテキスト化するための介入、条件、設定に基づいて、主要なメッセージを作成するために、レビュー全体でナラティブに合成されました。
BOX 1.包含および除外基準
包含基準:
レビューの種類:有効性の問題に焦点を当てた英語の系統的レビュー。質の高いエビデンスに焦点を合わせるために、研究の大部分(含まれるものの半分以上)または明確に報告されたサブグループは、ランダム化比較試験(RCT)でした。
母集団:高齢者(幅広いレビューから主要なメッセージを収集するために50年以上の試験での平均参加者年齢)、レビューの焦点または定義されたサブグループ、単一のLTCまたは複数の罹患率、または高齢者に共通の状態たとえば、虚弱、パーキンソン病、脳卒中、認知症、「入院のリスクがある」、または家族介護者を対象としたものなど、LTCの用語で通常カバーされない人々。
介入:プライマリまたはコミュニティの設定に基づいたケアモデルの全体的なトピックまたはサブグループ分析。
除外基準:
人口:若い成人でより一般的または専門的な管理が必要な状態(例:癌、ただしこれらの状態のいずれかに少数の研究が含まれていた場合、大多数の研究が関連していた場合はレビューを除外しなかった)人口(子供を含む)。
介入:明確に定義されたサブグループのない広範な介入を含むレビュー(例:非薬理学的介入のレビュー)、単一の介入(例:運動)、教育的または診断的介入、非介入的トピック、別の環境が主導する介入(例:在宅ケア) 。
レビューの種類:実装または経済的結果のみに焦点を当てたレビュー。
3結果
2,129のユニークなタイトルとアブストラクトのうち、178の全文がレビューされ、54の系統的レビューが含まれていました(図 1)。レビューには主に米国、カナダ、ヨーロッパの研究が含まれており、一部のレビューにはアジア(中国、香港、日本、インド、シンガポール)とオーストラリアの研究が少数含まれています。ほとんどのレビューは、多疾患併存(一般に長期的な身体状態とうつ病、n = 13)または1つ以上のLTC(主に糖尿病、COPD、心血管疾患およびうつ病、n = 12)を持つ人々を含む「LTC」の研究に焦点を当てました。認知症(n = 8)、フレイル(n = 7)、脳卒中(n = 5)、これらの組み合わせ(n = 4)、家族介護者(n = 3)、および入院のリスクがある人々(n = 2)。18件はより広範なレビューにおけるサブグループ分析であり、残りは全体のレビューでした。レビューは、含まれた試験の質を評価した。レビュー内およびレビュー間で、試験の質はさまざまであると報告されました。15件のレビューのみが、言語による研究の包含を制限しませんでした– 8件は少数の(通常はヨーロッパの)言語に制限されました。1つにはすべての言語が含まれますが、高所得国に限定された研究が含まれます。23件のレビューで、検索またはスクリーニングレベルの英語以外の論文が除外されました。そして、7人はこれを報告しませんでした。

4機能:ケアモデル
多数のプライマリーケアモデルとコミュニティベースのケアモデルが評価された。これらのモデルは、各モデルのレビューから得られた主要な知見とともに、表1に概説されている。多くのモデルは、その定義とコンポーネントがかなり重複しています。20件のレビューでは、コンパレータの詳細は報告されていません。報告された場合、比較グループは通常、通常のケアまたは強化/拡張された通常のケア(これらは元のレビューで合成にグループ化されることが多かったため、結果で言及される場合は「通常のケア」としてグループ化)で構成され、一部のレビューでは少数の研究が報告されました待機リストコントロールまたはより強度の低いケース管理を使用する。コンパレーターが報告された場合、これは結果で指定されます。報告されていない場合、これは不明確でした。すべてのモデルで、最も有望な効果は、メンタルヘルス(特に抑うつ症状)に関連しており、身体的転帰およびサービスの使用に対する決定的な効果はほとんどありませんでした。
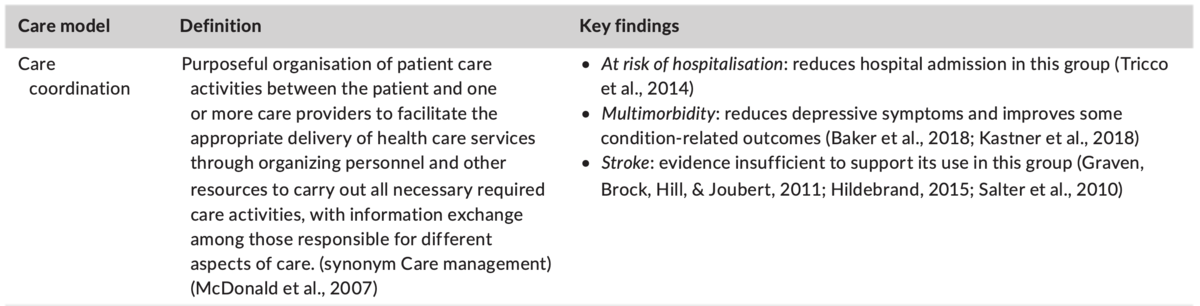
表1. ケアモデルと裏付けとなる証拠



|
ケアモデル |
定義 |
主な調査結果 |
|
Care coordination |
必要なすべての必要なケア活動を実行するための要員とその他のリソースを編成し、ケアのさまざまな側面の責任者間で情報交換を行うことにより、ヘルスケアサービスの適切な提供を促進するための、患者と1人以上のケアプロバイダー間の患者ケア活動の意図的な編成。(同義語のケア管理)(McDonald et al。、 2007) |
入院の危険性:このグループの入院を減らす(Tricco et al。、 2014) 多疾患併存:うつ病の症状を軽減し、いくつかの状態関連の転帰を改善します(Baker et al。、 2018 ; Kastner et al。、 2018) 脳卒中:このグループでの使用をサポートするにはエビデンスが不十分(Graven、Brock、Hill、&Joubert、 2011 ; Hildebrand、 2015 ; Salter et al。、 2010) |
|
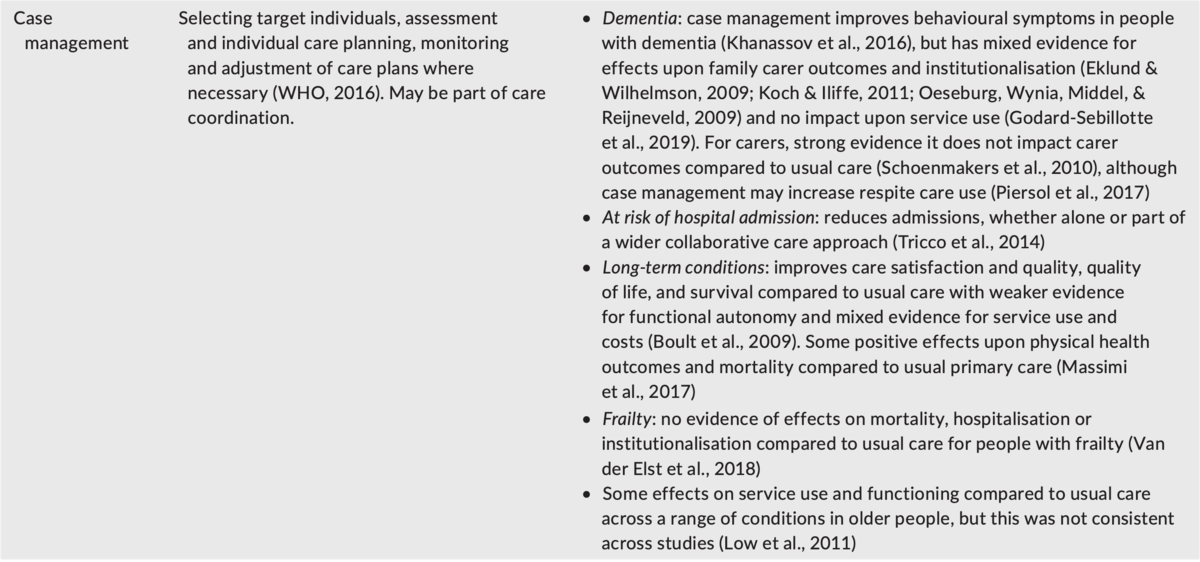
Case management |
対象となる個人の選択、評価と個人のケア計画、必要に応じたケア計画のモニタリングと調整(WHO、 2016年)。ケア調整の一部となる場合があります。 |
認知症:症例管理は認知症の人の行動症状を改善しますが(Khanassov et al。、 2016)、家族の介護者の転帰と施設への影響についてはさまざまなエビデンスがあります(Eklund&Wilhelmson、 2009 ; Koch&Iliffe、 2011 ; Oeseburg、Wynia、Middel 、&Reijneveld、 2009)およびサービスの使用への影響なし(Godard-Sebillotte et al。、 2019)。介護者については、通常のケアと比較して介護者の転帰に影響を与えないという強力なエビデンスがある(Schoenmakers et al。、 2010)が、ケース管理によりレスパイトケアの使用が増える可能性がある(Piersol et al。、 2017) 入院のリスクがある:単独でも、より広範な共同治療アプローチの一部でも、入院を減らす(Tricco et al。、 2014) 長期的な状態:通常のケアと比較して、ケアの満足度と質、生活の質、生存率が向上し、機能的自律性のエビデンスが弱まり、サービスの使用とコストのエビデンスが混合する(Boult et al。、 2009)。通常のプライマリケアと比較して、身体の健康転帰と死亡率にプラスの効果がいくつかあります(Massimi et al。、 2017) フレイル:虚弱者の通常のケアと比較して、死亡率、入院または施設への影響の証拠はない(Van der Elst et al。、 2018) 高齢者のさまざまな状態での通常のケアと比較して、サービスの使用と機能にいくつかの影響がありますが、これは研究間で一貫していませんでした(Low et al。、 2011) |
|
Shared care |
定期的な退院と紹介を超えた情報交換の強化を伴う、慢性疾患患者のプライマリケア医師と専門ケア医師による計画されたケア提供への共同参加(Smith et al。、 2017) |
長期的な状態:共有ケアは、通常のケアと比較してうつ病を改善しますが、生活の質や他の患者報告の測定にさまざまな影響を及ぼし、身体的健康の結果やサービスの使用にはほとんどまたはまったく影響しません(Smith et al。、 2017) |
|
Integrated care |
ライフコース全体にわたる多面的なニーズを満たすための質の高いサービスの包括的な提供の促進。さまざまな設定とケアレベルにまたがる調整された学際的なチームによって提供されます(WHO、 2016) |
長期的な状態:通常のケアと比較して、臨床転帰への影響は限定的であり、サービスの使用とプロセスへの影響はわずかである(Mitchell et al。、 2015) 脆弱性:通常のケアと比較したサービス使用への影響のエビデンスはまちまちです(Beland&Hollander、 2011年)。他の結果への影響なしまたは限定的(Berntsen et al。、 2019) いくつかの試験では地域社会および病院サービスの利用の増加に関連して、通常のケアと比較して混合集団の臨床転帰を改善しなかった(Low et al。、 2011) |
|
Chronic care model |
縦断的、予防的、コミュニティベースのアプローチで、通常、コミュニティ、医療システム、自己管理サポート、意思決定サポート、デリバリーシステム設計、臨床情報システムなどの6つのコンポーネントが含まれます(WHO、 2016年)。 |
フレイル:通常のケアと比較して転帰への影響は少ない(Hopman et al。、 2016) 多疾患併存:通常のケアと比較してメンタルヘルス関連の転帰を改善しますが、HbA1cレベルへの影響についてはエビデンスが混在しています。現在、死亡率または生活の質への影響を示すエビデンスはない(Hopman et al。、 2016 ; Lemmens et al。、 2015) 脳卒中:健康関連の生活の質を改善しますが、抑うつ症状や社会参加は改善しません(Graven et al。、 2011) |
|
Collaborative care |
集学的アプローチ、通常は学際的なアプローチ、ケアのエビデンスに基づくケアプロトコル、強化された薬理学的および心理学的介入、予定されたフォローアップ、および定義された専門職間コミュニケーションシステムを含む統合ケアモデルに基づきます。通常、ケースマネージャーがこの中核的な役割を担っています(Ekers et al。、 2013)。 |
鬱病と糖尿病の併存症:通常のケアと比較して鬱病の症状(Atlantis et al。、2014 ; Huang、Wei、Wu、Chen、&Guo、2013)とHbA1c(Atlantis et al。、 2014)を 改善し ます うつ病とLTCのある人; 通常のケアと比較して抑うつ症状を改善し(van Eck van der Sluijs et al。、 2018 ; Ekers et al。、 2013 ; Watson et al。、 2013)、身体的転帰と身体的および精神的疾患の重荷の結果に対する軽度から中程度の影響(van Eck van der Sluijs et al。、 2018)とメンタルヘルス関連の生活の質(Watson et al。、2013)への影響 うつ病のみの人よりも、うつ病と身体のLTCの方が効果サイズが大きい(ただし、LTCの数によって変化しない)(Panagioti et al。、 2016) うつ病を患う虚弱高齢者:通常のケアと比較してメンタルヘルスの結果にはさまざまな影響があるが、身体機能やサービスの使用には影響がない(Frost、Bauernfreund、&Walters、 2019) 冠状動脈性心疾患とうつ病の人:通常のケアと比較して、メンタルヘルスの結果と主要な心臓の有害事象の短期的なリスクを改善します(Tully&Baumeister、 2014年) |
|
Other |
看護師主導の介入は、フレイルなサービスの使用に混合効果をもたらし(Liebel et al。、 2009)、LTCの精神機能(活力、社会的および感情的機能、精神的健康を含む)を改善しますが、他の結果(Amo-Setien et al。 、 2019)そして、脳卒中のうつ病には影響しません(Salter et al。、 2010) 学際的なプライマリケア(プライマリケアプロバイダーと1人以上の他の医療専門家)が、通常のケアと比較して生活の質、機能的自律性、およびサービスの使用を改善するという限られた証拠(Boult et al。、 2009) 通常のケアと比較して、認知症におけるサービス利用(Godard-Sebillotte et al。、2019)または脳卒中ケアにおける日常生活活動(Fens et al。、2013) に対する影響を示した幅広い介入モデルはありません 予防的家庭訪問は、通常のケアと比較して、健康とサービスの使用におけるいくつかの改善と関連していましたが、他の結果とは関連していませんでした(Boult et al。、 2009) 慢性状態での予防的なリハビリは、通常のケアと比較して機能を改善しますが、サービスの使用は改善しません(Boult et al。、 2009) 多くの研究から得られた通常のケアと比較した、うつ病とLTCの段階的ケアに関する混合証拠(Maehder et al。、 2019) 脳卒中に対する家族支援組織の介入(二次予防のためのアドバイス、情報、感情的サポートおよびライフスタイルの変更、退院計画中のリハビリチームとの連絡)は、抑うつ症状に違いを生じなかった(Salter et al。、 2010) LTCsのためのパーソナライズされたケア計画は、いくつかの物理的な健康アウトカムとうつ病ではなく、生活の質に通常のケアに比べて小さい正の効果と関連していた(コールターら。、 2015) 消費者主導型ケアは、通常のケアと比較して臨床転帰にほとんど影響を与えませんでしたが、さまざまな状態の高齢者の満足度とコミュニティサービスの利用を改善しました(Low et al。、 2011) 一般の医療従事者による慢性疾患の管理は、一般的な健康や生活の質に影響を与えませんでしたが、身体的な健康の結果を改善する証拠は限られていました(Carr et al。、 2011) |
ここで紹介したモデルを簡単に紹介
Care coordination
https://www.ahrq.gov/ncepcr/care/coordination/atlas/chapter2.html

患者/家族の視点、医療専門家の視点、システム担当者の視点の3つに分かれる
図の中央には、ケア調整の中心的な目標が示されています。色付きの円は、参加者、設定、およびケアの経路とワークフローにとって重要な情報の一部を表しています。色付きの円を結ぶ青いリングは、ケア調整です。つまり、ケア経路に沿ってギャップ(空白)を埋める方向で連携をしていきます。
Case management
https://www.miccsi.org/wp-content/uploads/2017/03/CMSA-Standards-2016.pdf
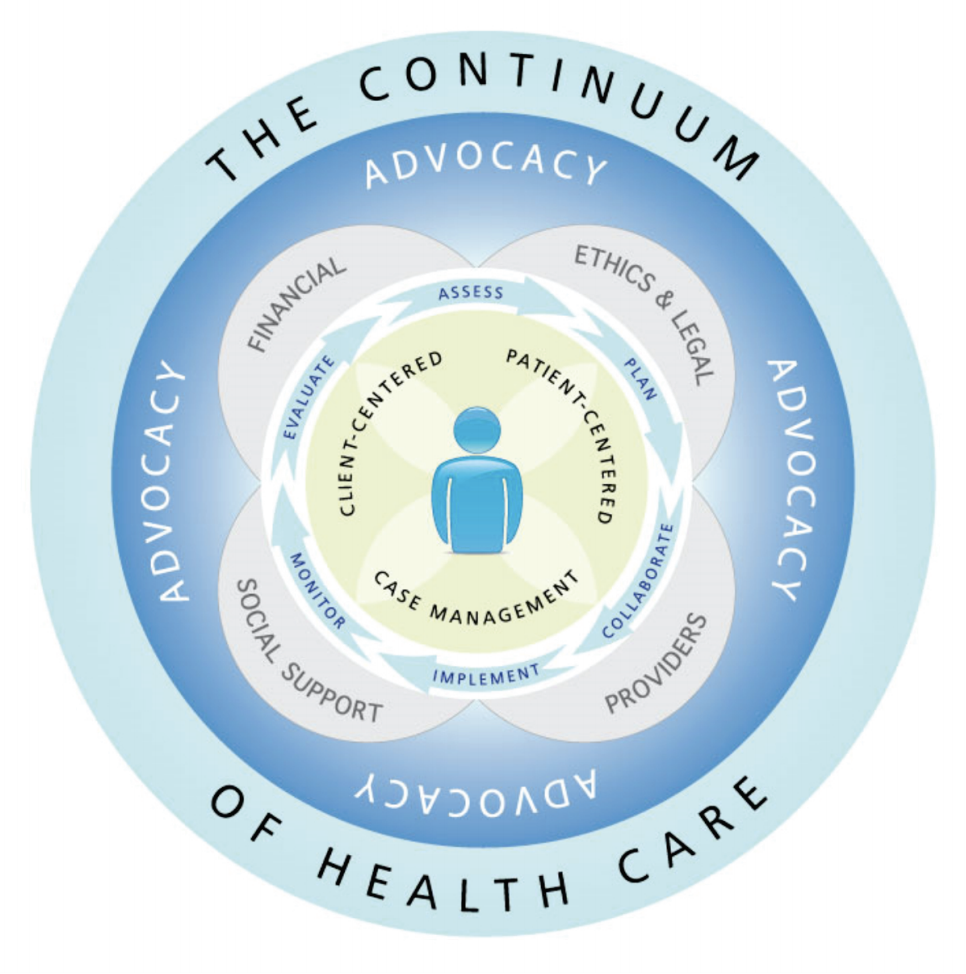
https://www.ijic.org/articles/10.5334/ijic.2477/
症例発見、信頼関係の確立、評価、計画、ナビゲーション、ケアの提供、実装、コーディネーション、モニタリング、評価、フィードバック、教育/情報、擁護、協力的なカウンセリング、管理、排出/解放、コミュニティサービスの開発がコンポーネントになり、さまざまな健康状態のさまざまなコンテキストでのヘルスケアとソーシャルケアの調整、統合、および管理を引き続きサポートします
Shared care
https://www.liberaldictionary.com/shared-care/
シェアードケアは、イギリスのヘルスケアとソーシャルケアで広く使用されている用語です。シェアードケアは、専門家と素人の間のパートナーシップの確立を含み、そこで彼らは共通の目標を共有します。例としては、患者の健康状態の改善が挙げられます。これは、社会的サービスと外部の一般提供者の共同の取り組みによって不利な立場にある人の生活が改善される、大きな責任のあるケアと手配を行う患者のエンパワーメントがあります。真に共有されるケアでは、パートナーシップは真に同等であり、どちらのパートナーも従順でも優越でもありません。
Integrated care

地域包括ケアの理論的基盤の概念として藤沼先生も紹介しています。
4つの統合(Functional integration:機能的統合、Organizational integration:組織的統合、Professional integration:専門的統合、Clinical integration:臨床的統合)
5つの統合のタイプ(Systemic integration:システム統合、Normative integration:規範的統合、Organizational integration:組織的統合、Administrative integration:管理的統合、Clinical integration:臨床的統合)
統合の場も2種類あり
Vertical integration:垂直的統合(1つの組織でおこなう)
Horizontal integration:水平的統合(様々なケアの連携を改善)
という軸を理解してアプローチする概念です。
Collaborative care
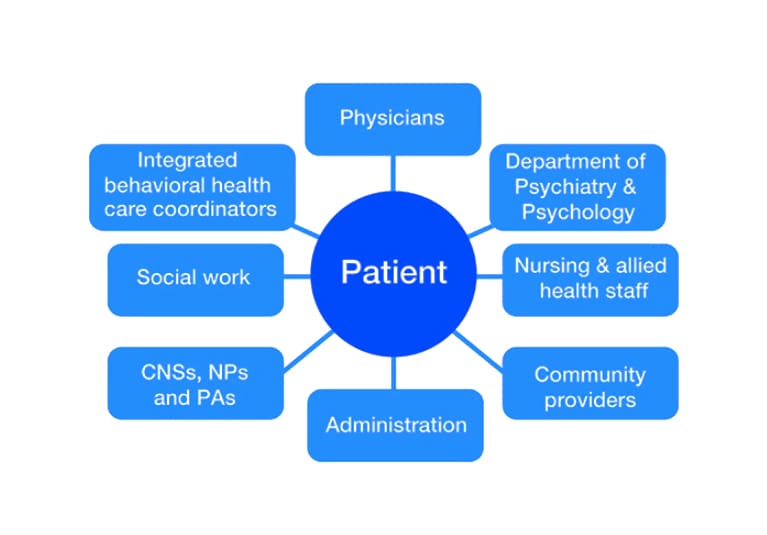 2010年、NEJMでのワシントン大学の研究は、うつ病と共存する糖尿病または心血管疾患の患者の転帰と生活の質を改善する共同ケアモデルについて説明しました。ケアコーディネーター。通常は登録看護師であり、毎週患者さんと会って状態を監視し、サポートと積極的なフォローアップを提供し、毎週ケアコーディネーターと一緒に問題のケースをレビューし、主治医に治療の推奨を行うコンサルティング精神科医および主治医プロバイダーがいます。コンピュータ化されたレジストリ、継続的なデータ分析、品質改善などを行う仕組みです。
2010年、NEJMでのワシントン大学の研究は、うつ病と共存する糖尿病または心血管疾患の患者の転帰と生活の質を改善する共同ケアモデルについて説明しました。ケアコーディネーター。通常は登録看護師であり、毎週患者さんと会って状態を監視し、サポートと積極的なフォローアップを提供し、毎週ケアコーディネーターと一緒に問題のケースをレビューし、主治医に治療の推奨を行うコンサルティング精神科医および主治医プロバイダーがいます。コンピュータ化されたレジストリ、継続的なデータ分析、品質改善などを行う仕組みです。
Chronic care model
慢性ケアモデル(CCM)は、プライマリケアにおける慢性疾患患者の長期ケアと健康を改善するためのフレームワークです。
子宮内膜症に対して、婦人科医、統合医療、メンタルヘルス、鎮痛剤、専門外科医、理学療法、消化器科、泌尿器科、プライマリケアが関わる例を示しています。

骨粗鬆症にモデルに当てはめた青木先生のポートフォリオもありました。
ざっくりとモデルを復習した上で、エビデンスをまとめてみましょう。
5機能するもの:理論的根拠
あるレビューでは、理論的根拠を持つことは、対照群と比較して、LTCの看護介入における精神機能の改善と関連していた(詳細は報告されていない;効果量= 0.331、95%CI 0.186–0.476、n = 13)理論に基づいていると報告されました(Amo-Setien et al。、 2019)。自己管理モデル、脆弱性の理論、Banduraの自己効力理論などの一連の理論が一次研究で報告されました(Chow&Wong、 2014 ; Markle-Reid et al。、2006)。特定の理論が最も効果的であると強調されていません。
6機能:介入目標
6.1特定の結果をターゲットにする
介入のターゲットが明確で特定の結果であることは、対照と比較して対応する結果の改善に関連していた(ほとんどの試験で通常のケア)(Baker、Grant、&Gopalan、 2018 ; Reilly et al。、 2015 ; Smith et al。 、 2016)、例えば、制度化を遅らせ、うつ病を軽減する。目標に関係なく通常のケアと比較して結果が混合された段階的ケア以外(Maehder et al。、 2019)。より広い目標(例えば、自律性に焦点を合わせた特定の疾患のリスクと合併症の制御)は、結果がまちまちだった(Boult et al。、 2009 ; Morilla-Herrera et al。、 2016)。
6.2リスクのある集団を対象とする
ベースラインの罹患率が高い人をターゲットにすると、LTCの通常のケアと比較して入院が減少し(Smith et al。、 2017)、患者から報告された転帰が改善された(Baker et al。、 2018)。医療サービスの高い利用者をターゲットにすると、サービス利用の結果はまちまちでした(Baker et al。、 2018 ; Tricco et al。、 2014)。
7機能:ケアのコンポーネント
7.1自己管理
自己管理に明確に焦点を当てていることは、LTCと多疾患併存のポジティブな臨床転帰に貢献しました(Kastner et al。、 2018 ; Reynolds et al。、 2018)、LTCのソーシャルサポート(通常のケアと比較して)(Reilly et al。、 2015)、そして入院のリスクがある高齢者の入院を減らす(Tricco et al。、 2014); 認知症患者の急性期病院での通常のケアに対する症例管理の有効性には影響しませんでした(Godard-Sebillotte、Le Berre、Schuster、Trottier、およびVedel、 2019)。
7.2評価と予防的ケア
情報提供による評価や積極的な管理(推奨や紹介ではなく特定の指定医療専門家が講じた措置)を含むケアのモデルでは、通常のケアと比較して、高齢者の老人ホームへの入院が減少しましたが、機能やサービスの使用には影響がありませんでした(Beswick 、Gooberman-Hill、Smith、Wylde、およびEbrahim、 2010)。アクティブな手順(創傷ケア、検体採取、抵抗運動、処方薬などの症状の予防または緩和に関連する技術活動)を含めると、LTCの看護師主導のケアモデルでは、教育、指導、カウンセリングに比べて精神機能に大きな影響がありました(Amo‐Setien et al。、 2019)。ケア計画にフレイルな患者が関与していることが判明した1件のレビューの1つの試験では、より肯定的な結果が得られました(Eklund&Wilhelmson、 2009年)。
7.3患者教育
患者に提供される教育の種類が詳細に報告されることはめったにありませんが、結果への影響については相反するエビデンスがありました。自己管理とともに多病的状態のケア調整介入に含まれる場合、サブグループ分析では、通常のケアと比較してうつ病とHbA1cに影響が見られましたが、メンタルヘルスサービスの使用が増加しました(Kastner et al。、 2018)。入院のリスクがある人では、患者教育により入院が減少しました(Tricco et al。、 2014)。しかし、教育を含む介入特性は、通常のケアと比較して、認知症の人々の急性期病院サービスの使用に影響を与えませんでした(Godard-Sebillotte et al。、 2019)。看護師主導の介入で患者を教えることは、LTCの精神機能(活力、社会的および感情的機能、精神的健康を含む)に影響を与えませんでした(Amo-Setien et al。、 2019)。
7.4心理的サポート
うつ病と糖尿病の心理的サポートを提供することに主眼を置いた共同医療介入(Ekers et al。、 2013)およびモニタリングに加えて共同医療モデルが心理療法を提供したもの(van Eck van der Sluijs et al。、 2018)も同様の効果をもたらした病気の負担と身体的および精神的健康に関するメタ分析の通常のケアと比較したサイズを、そうでないものと比較しました。
7.5ライフスタイル管理
二次的脳卒中予防のためのライフスタイル管理介入は、全体的な試行回数は限られていたものの、ポジティブなライフスタイルの変化(例:身体活動)を生み出し、生活の質を改善し、血圧などの身体的健康の結果を改善するのに効果的でした(Lawrence et al。、 2012) 。ライフスタイルのリスク要因を対象とした研究を削除すると、通常のケアから非有意性へのケアと比較して、うつ病とHbA1cへの影響が減少しました(Atlantis、Fahey、&Foster、 2014)。
7.6投薬管理
通常のケアまたはより強度の低い症例管理と比較して、薬物治療を含むまたは除外する症例管理介入の間のサービス使用に違いはありませんでした(Tam-Tham et al。、 2013)。
7.7介護者のサポート
介護者のサポートを含めることは、介護施設の移動の遅延と、LTC患者の通常のケアと比較して生活の質の向上と関連していた(Boult et al。、 2009)。
7.8コンポーネントの組み合わせ
5つのレビューで、さまざまな要素の組み合わせについて検討しました。多数の異なるコンポーネントを含む包括的なアプローチは、LTCのHbA1cを低減するのにより効果的であり(Coulter et al。、 2015)、フレイルの障害への影響がより大きくなりました(Liebel et al。、 2009)。ただし、モデル全体で3つのコンポーネントの天井効果があるように見えました(Ekers et al。、 2013 ; Reynolds et al。、 2018)。最大の潜在的影響は、患者サポート(自己管理および/または教育)、専門家サポート(明確なケア経路および/または意思決定サポート)、および何らかの形のケア調整(例:ケース管理)(Coulter et al 。、 2015 ; Kastner et al。、 2018 ; Reynolds et al。、 2018)。
8効果:介入の強度
介入の強度は、レビュー全体でどのように定義されたかで大きく異なり、比較可能性を制限しました。7件のレビューで純粋に頻度で定量化し、高強度を3か月以上の月に1回以上の接触(Coulter et al。、 2015)、週に6回以上の対面接触(Fens et al。 、 2013)、6回以上の訪問(Hildebrand、 2015)、12か月あたり14.4回以上の連絡(Backhouse et al。、 2017)または1か月以上の訪問(Baker et al。、 2018); 1つはメタ回帰のセッション数を使用しました(Ekers et al。、 2013)。3つのレビューでは、学際的な情報、予定された訪問の数、および期間に応じて強度をスコア付けしました(Beswick et al。、 2010)およびケースロード、患者の複雑さ、訪問の頻度、提供されるサービスの範囲(Corvol et al。、 2017)または18の異なる基準の組み合わせ(Somme et al。、 2012)。最終レビューでは、著者の主観的判断を使用しました(Low et al。、 2011)。
介入の強度は有効性にさまざまな影響を及ぼし、レビューで一部の条件と結果への影響を示したが、他の影響は示さなかった。通常のケアと比較して、より強力な介入は脆弱性にほとんど影響を与えないようでした(Beswick et al。、 2010)。しかし、介護者、混合型LTCおよび脳卒中後の高齢者の場合、強度が高いほど、HbA1cレベル(Coulter et al。、2015)、生活の質(Fens et al。、 2013)、健康に対する通常のケアよりも効果が高かった 関連する生活の質、うつ病と不安症(ヒルデブランド、 2015年)、介護者の結果(Corvol et al。、 2017年)、および全体としてより肯定的な結果(Low et al。、 2011年))。認知症の証拠は相反しており、入院、施設化、または死亡率への影響は見られず(Backhouse、Dickens、Richards、およびMcCabe、 2015)、臨床転帰に対するいくつかのプラスの影響(Somme et al。、 2012); そして、うつ病に複合的な影響があった多疾患併存について(Baker et al。、 2018 ; Ekers et al。、 2013)。定義や条件によって大幅に異なるため、複雑な条件の高齢者にとってより強力な介入がより有益であるかどうかについて、明確な結論を出すことはできません。
介入期間の長さの影響は、LTCの転帰タイプによって影響を受けた。より短い介入はより良い精神機能スコアにつながりました(Amo-Setien et al。、 2019); より長い介入はHbA1cレベルを改善しましたが、血圧は改善しませんでした(Berntsen et al。、 2019)。認知症におけるより長い症例管理介入は施設化の減少と関連していたが(Pimouguet et al。、2010)、通常のケアと比較して他のケアモデルでは関連して いなかった(Godard-Sebillotte et al。、 2019)。
9機能:スタッフの配置
9.1特定の専門的役割
看護師の役割に焦点を当てた研究の最大量。さまざまな専門家による介入の提供を直接比較したものはほとんどありません。一連の結果全体で、LTCおよび認知症管理における看護師主導のプライマリケアとプライマリケアの医師およびソーシャルワーカーとの間には、有意差はほとんどありませんでした(Backhouse et al。、 2015 ; Health Quality Ontario、 2013b ; Pimouguet et al。、 2010 ; Somme et al。、 2012)。資格があり、訓練を受けた経験豊富な看護師は、フレイルの障害のより良い結果と関連し(Liebel et al。、 2009)、LTCの拡張期血圧と収縮期血圧およびHbA1cを減少させました(Massimi et al。、 2017))。訓練を受けたケースマネージャーは、1つのレビューで成功した統合的介入の重要な要素でした(Oeseburg、Wynia、Middel、Reijneveldなど、 2009年)。
他の医療専門家に関しては、ソーシャルチーム(Stokes et al。、2015)、患者ナビゲーター(Tricco et al。、2014)、医師との直接接触(Beswick et al) をケアチームに含めても、アウトカムにはほとんど影響がないという証拠が示されました al。、 2010)および作業療法士(OTs)(Hildebrand、 2015)。専門職のタイプによって影響を受ける唯一の結果は、うつ病に対する潜在的な影響と、脳卒中におけるOT主導の症例管理による休息サービスの利用の増加(Hildebrand、 2015 ; Piersol et al。、 2017)と薬剤師を含めることによるコストの削減(Kane&Shamliyan、 2011年)。チームの組み合わせでは、通常のケア(van Eck van der Sluijs et al)と比較して、医師や精神科医と協力しているケースマネージャーと比較して、GPと協力しているケースマネージャーによって提供される共同ケアで、病気の負担や身体的または精神的健康の結果に違いはありませんでした。 al。、 2018)。同様に、医師のタスクを別の医療従事者に置き換えると、機能、生活の質、コスト、および罹患率にいくつかの改善が見られましたが、チームのタイプと結果に明確なパターンはありませんでした(Kane&Shamliyan、 2011)。
9.2学際的なチーム
プライマリーケアにおける学際的なアプローチが転帰を改善する可能性があるという限定的かつ混合的なエビデンスがありました(Boult et al。、 2009 ; Liebel et al。、 2009 ; Smith et al。、 2016 ; Tricco et al。、2014)。 LTCの生活の質と機能的自律性(Boult et al。、 2009)および入院のリスクのある患者の入院の減少(Tricco et al。、 2014)。あるレビューでは、患者の臨床転帰ではなく、ケアプロセスのみに影響がある可能性があると結論付けました(Kane&Shamliyan、 2011)。MDTで管理されている患者の死亡率と自己評価による健康の短期的な改善を除いて、MDTのケース管理と単一のケースマネージャー(通常のケアまたはケース管理なしの場合と比較)の効果サイズにはほとんど違いがありませんでした(Stokes et al。 、 2015)。チームの構成は大幅に異なり、MDTのアプローチは、組織の変更など、より広い見出しの下に含まれることがあったため、このトピックのレビューから明確な結論を導き出すことはほとんどできませんでした。
9.3統合
チームの統合は、構成よりも重要であるように見えました。ケースマネージャーの統合の拡大は、患者ケアチーム内のリンクに従って分類された認知症の人々のケアの質の向上と、急性および長期のケア構造の拡大(Somme et al。、 2012)と、物語の場合の虚弱の結果の改善に関連していたケースマネージャーと他の種類のケアとのつながりに基づいて統合が評価された場合、認知症の人の介護者には当てはまりませんが、ケースマネージャーと医療従事者の間の良好なコミュニケーションと緊密な協力として評価されました(Oeseburg、Wynia、Middel、&Reijneveld、 2009)。 Corvol et al。、 2017)。統合型糖尿病ケアとして記述されている研究をメタアナリシスから除外すると、協調型糖尿病とうつ病ケアにおけるうつ病とHbA1cレベルに影響はありません(Atlantis et al。、 2014)。
9.4コミュニケーション
患者と母集団のデータを整理する臨床情報システムはいくつかの研究で検討されていますが、これらは専門家と患者の利益を示し、証拠と患者のニーズに基づく意思決定支援は専門家の結果を改善しますが患者の改善はしません(Reynolds et al。、 2018)。
9.5電子サポート
LTCの場合、ケア調整のeツールは、通常のケアと比較して、結果にさまざまな影響を及ぼしました。入院、滞在期間、および救急診療科への好影響を示した唯一の試験は、ガイドラインにリンクされたPCPの電子ラボレポートでした(Health Quality Ontario、 2013a)。この分野の研究は非常に限られていた。通常のケアと比較して、シェアードケアLTC介入の限られた範囲の結果に対するテクノロジーのいくつかの有望な影響があり、主に電子意思決定支援(喫煙とアスピリン遵守への影響に限定)、シェアされた電子医療記録(サービスの使用には影響なし)ケアプロセスと健康状態の改善)およびITプラットフォーム(一部の知識と健康状態の改善)(Kooij et al。、 2017)。
9.6配達
うつ病とLTCの共同ケアでは、一部の対面フォローアップと電話のみのフォローアップを使用した研究間で、通常のケアと比較して効果の大きさに有意差はなかった(Ekers et al。、 2013)。高齢者の共同ケアモデルに遠隔メンタルヘルスを追加すると、通常のケアと比較して抑うつ症状と生活の質が改善することがわかりましたが、評価されたのは1つの研究のみです(Gentry&Lapid、 2019)。
10エビデンスの要約
ケアのモデルには重複する構成要素が含まれており、状態に関係なくうつ病の症状やその他のメンタルヘルスの結果にプラスの影響を与える可能性が最も高いことを示唆する強力なエビデンスベースがありました。これは、うつ病とLTCの介入を対象とした多数のレビューを部分的に反映している可能性があります。明確なターゲットによる介入は、ターゲットの結果に影響を与える可能性が高く、明確な理論的基盤を持つ介入は、精神機能の改善に効果的である可能性が高かった。自己管理、患者教育、フォローアップケア手順による評価、構造化されたケアプロセスまたは経路を含む介入は、さまざまな臨床転帰を使用した有効性のより大きな証拠と関連していた。3つ以上のコンポーネントを含むものは、より効果的であるとは思われませんでした。人材配置に関しては、統合のレベルは特定の医療専門家よりも重要であるように見えました。より高度な資格と経験豊富な看護師は、より良い結果と関連していた。
より弱い証拠は、介護者のサポートが長期ケアへの移行を減らし、生活の質を改善する可能性があり、ライフスタイル管理が一連の臨床転帰の改善に効果的である可能性があることを示唆しました。現在のエビデンスでは、心理的サポートと投薬管理は、それぞれ臨床転帰とサービス利用の有効性を改善するようには見えません。優れた臨床情報システムがあり、これをサポートするテクノロジーを使用することも、より良い結果に関連する可能性があるという弱い証拠がありました。
11他の文献との比較
統合ケアモデルの一般的な要素には、集学的チームケア、包括的な評価、ケース管理が含まれ、多くの介入はマイクロレベルのサービス変更に焦点を当てています(Briggs et al。、 2018)。ある現実主義者のレビューは、包括的ケアへの構造化されたアプローチの使用、正式なプロバイダーの役割の確立、MDT管理による複数の状態への対処、特定のコミュニケーションプロセスの提供を通じて、ケア調整介入が機能する可能性が高いことを示唆しています(Kastner et al。、 2019)。私たちのレビューは、専門家へのサポート(トレーニング、意思決定支援など)、構造化された共同ケアプロセス、統合ケアの必要性を確認しています。コロケーション、統合された情報システム、チームがサービスに関与していることをスタッフに感じさせる単純な魅力的なビジョン、役割とコラボレーションのルールの明確な概要、優れたリーダーシップを通じて、チームレベルでより優れた統合が達成される可能性があります(Threapleton et al。、 2017)。小規模で焦点を絞ったチームは、統合ケアの実装を促進するだけでなく、統合を可能にする価値観/目標、ポリシーとガバナンスの共有を促進すると考えられています(Threapleton et al。、 2017)。
理論的根拠は有効な要素として強調されていましたが(Amo-Setien et al。、 2019)、Amo-Setien et alの研究には幅広い理論が報告されており、特定の理論の使用を裏付ける証拠はありません。自己管理アプローチおよび疾患管理における患者の優先順位に焦点を当てることも、現実主義的レビュー(Kastner et al。、2019)でケア調整介入の主要な側面として強調されました が、これらはケアのモデルではあまり注意が払われていない(Briggs et al。 、 2018)。私たちのレビューは、特に抑うつ症状への影響において、自己管理、患者教育、潜在的に介護者のサポート、ライフスタイルの変化など、患者レベルの要素を明確に強調する必要性を強調しました。ただし、このレビューではほとんどの介入が機能または生活の質に一貫した明確な影響を及ぼしました。これは、ケアモデルがこれらの結果に利益の明確な証拠があるコンポーネントを除外しているためである可能性があります。認知症を伴う家の改造(Gine-Garriga、Roque-Figuls、Coll-Planas、Sitja-Rabert、&Salva、 2014 ; Laver et al。、 2016 ; Stark et al。、 2017)。
12制限
このレビューで提示された証拠は、主に米国を中心とする高所得の西欧諸国に由来しています。含まれているレビューの大部分には、少なくともいくつかの言語制限があり、出版バイアスにつながる可能性があります。これらの介入の一部に必要なシステムレベルの変更を考えると、それらは他の設定、特に保険ベースのシステム以外の設定にうまく変換できない場合があります。チームの変更、アクティブな手順などの一部の概念は、含まれているレビューで必ずしも明確に説明されていませんでした。通常、レビューは、構成要素に応じて介入の有効性をいかにうまく分析するかが制限されていました。さらに、この最先端のレビューに含まれるレビュー内の有効性に関する結論を導くために使用されるプロセスは、(サブグループのメタ分析やメタ回帰ではなく)投票数と十分な一次研究報告に大きく依存する場合がありました。介入が意図したとおりに実施されたかどうかに関するプロセスデータを明示的に分析したレビューはほとんどありません。
このレビューには明確な制限があります。含まれるレビューや試験の質は評価しませんでした。これは最新のレビューでは通常の手順ではありませんが、一部のレビューは他のレビューよりも明らかに高品質でした。また、レビューが要約しているソーストライアルにはかなりの重複があり、現在利用可能なエビデンスベースをカバーしているという確信を裏付けていますが、一部のトライアルは二重にカウントされた可能性が高いです。レビューの概要を実施していないため、試験の重複を正式に評価しませんでした。重要なメッセージを抽出するために、レビューの大部分または明確なサブグループが私たちの研究の質問に焦点を当てた、より広範な研究または条件を含むレビューを含めました。レビューは必ずしも介入特性または主要な研究データを明確に報告したわけではなかった、いくつかの比較を困難にします。関心のあるトピックは、これらのコンポーネントが単独ではなく幅広い介入の一部として機能する方法であったため、個々のコンポーネントのレビュー(薬物療法のレビューや自己管理など)は含めていません。しかしながら、これは私たちの能力を制限し、これらのコンポーネントについての明確な推奨を行いました。結論は、LTC(van Eck van der Sluijs et al。、 2018 ; Ekers et al。、 2013 ; Massimi et al。、 2017)。
13将来の研究の方向性
疾患固有のアウトカム(例えば、HbA1cを測定した多くの研究)や、機能や生活の質などの複数の罹患率により広く適用できるアウトカム(Ferrucci et al。、2004)を対象とした協調的介入の設計 が必要です。さらなる研究の余地がまだある分野には、テクノロジー、介入の長さ、強度、チーム構成の最適な役割が含まれます。理学療法やOTなどの分野が機能的自立などの結果に重要な影響を与える可能性があるため、さまざまな専門家、特に非看護専門家を直接比較することも価値があります(たとえば、一部のOT主導型介入は有効性の見込みを示します; Smallfield&Heckenlaible、 2017)。新しい介入には、可能な場合は有効性の証拠がある構成要素を含め、構成要素の組み合わせの影響をより詳細に調査する必要があります。複雑なプライマリおよびコミュニティケア介入の将来の分析を促進するには、より明確な介入コンポーネントレポートと一貫した結果測定が必要です。
14結論
現在、多くのコンポーネントを共有し、同様の結果に影響を与えていますが、ほとんどのモデルは特定の疾患に焦点を当てています。このレビューは、多病的状態のケアの統合モデルに焦点を合わせる動きが、特にモデルに理論的根拠がある場合、抑うつ症状の軽減などの通常のケアに比べていくつかのプラスの効果をもたらす可能性が高いことを示唆しています(患者教育、自己管理を含む)構造化された専門家間のコラボレーションと専門家によるサポート)、罹患率の高い人を対象としています。
まとめ
既存の疾患管理モデルを多疾患併存やフレイルなどの高齢者に当てはめた研究のレビューでしたが、徐々に研究結果が揃ってきて感心させられます。まだエビデンスの集積は必要ですが、精神面でプラスになる以外の可能性を秘めていて興味深いですね。
総文字数:23490文字 普段も長いですが、今回はとびきり長かったですね。
最後まで読んでいただきありがとうございました。